2.9. L’ANTIBIOTHERAPIE
Il s’agit de l’usage des antibiotiques pour traiter les infections bactériennes prouvées ou suspectées ou pour prévenir une infection. (antibioprophylaxie)
Mauvais usage courant des antibiotiques
- Traitement des infections non bactériennes : Certaines infections virales sont traitées par des antibiotiques alors qu’ils n’ont pas d’effet sur les virus. C’est notamment le cas des infections des voies respiratoires hautes et certaines infections digestives (surtout chez les enfants).
Fièvre : toute fièvre n’est pas d’origine infectieuse bactérienne :
- Fièvre de courte durée : plusieurs infections virales ou parasitaires (y compris le paludisme peuvent en être responsable. Il faut donc bien poser le diagnostic avant de mettre en route un traitement antibiotique.
- Fièvre de longue durée (fièvre d’origine indéterminée, FOI) : ici aussi les infections bactériennes ne sont pas les seules pourvoyeuses de FOI.
- Posologie incorrecte : un dosage exagéré peut conduire à des effets indésirables parfois graves tandis qu’un dosage insuffisant conduit à l’inefficacité avec risque d’émergence de souches résistantes. De même une trop longue durée de l’antibiothérapie augmente le risque d’émergence de souches résistantes.
- Antibiothérapie seule sans mesure chirurgicales : les infections compliquées d’abcédation, présence de tissus nécrotiques ou de corps étranger ou d’obstruction canalaire ne peuvent pas se traiter par des antibiotiques seuls : il faut y associer des actes chirurgicaux (traitement de la porte d’entrée pour un sepsis, évacuation de pus, ouverture de canal obstrué etc.)
- Manque d’information bactériologique suffisantes : dans nos pays pauvres, l’antibiogramme est rarement disponible : l’antibiothérapie est souvent probabiliste, ce qui peut conduire à des erreurs. Une antibiothérapie adaptée au germe en cause est la règle, mais en l’absence d’information, il est utile de conduire correctement l’antibiothérapie probabiliste.
Bonne pratique de l’antibiothérapie
La prescription antibiotique doit prendre en compte:
- Les effets de l’antibiotique sur un patient donné (effet thérapeutique, effets indésirables)
- Les effets de l’antibiotique sur l’écologie bactérienne de l’environnement avec ses conséquences pour la collectivité.
La mise en route d’un traitement antibiotique nécessite de se poser les 9 questions suivantes :
1. Faut-il prescrire un antibiotique ?
Il est utile de s’assurer que l’infection est d’origine bactérienne en posant correctement le diagnostic. Toute pathologie fébrile n’est pas nécessairement bactérienne.
- Fièvre non infectieuse : cancer, fièvre médicamenteuse…
- Fièvre infectieuse non bactérienne : paludisme, infections virales.
NB : toute hyperleucocytose à prédominance neutrophilique ne signifie pas infection bactérienne. Les états de stress, de nécrose tissulaire peuvent donner lieu à une hyperleucocytose à présominance neutrophilique.
2. Faut-il un prélèvement bactériologique préalable ?
Dans nos milieux, le prélèvement bactériologique pose un certain nombre de problèmes, notamment la possibilité de faire la culture et antibiogramme. Néanmoins il est utile de se rappeler que dans certaines circonstances, le prélèvement bactériologique est inutile car la clinique seule oriente vers l’agent causal : les symptomes en rapport avec le Rumatisme articulaire aigu RAA suggère un seul germe : le streptocoque beta hémolytique.
Dans d’autres situations, le prélèvement peut se faire mais ne doit pas retarder l’antibiothérapie (sepsis grave) ; il est alors recommandé de commencer le traitement par un antibiotique à large spectre (ou association d’antibiotiques) et réajuster le tir après obtention des résultats de la culture/antibiogramme. Le réajustement devra viser la désescalade antibiotique en préférant l’antibiotique efficace ayant le spectre le plus étroit pour limiter le risque de développement des souches multirésistantes.
Dans certaines circonstances, la culture/antibiogramme sera indispensable (infection nosocomiale, échec d’une première antibiothérapie…)
3. Quel antibiotique choisir ?
Le choix dépendra évidemment
- de l’agent causal (supposé ou confirmé),
- de l’état du patient, et
- des propriétés de l’antibiotique notamant sa pharmacocinétique, et son spectre. La cinétique de l’antibiotique doit lui permettre d’atteindre le site infectieux à des concentrations supérieures à la CMI ; le spectre informe sur les bactéries sensibles à cet antibiotique. Si l’agent causal est connu, il doit figurer dans le spectre de l’antibiotique choisi.
L’agent causal peut être supposé en tenant compte
- de la clinique : par exemple, une angine rouge suggère le streptocoque beta hémolytique comme agent causal !
- de l’écologie habituelle du tissus infecté et de l’hôpital, et
- du spectre négatif d’une antibiothérapie antérieure.
4. Faut-il une association d’antibiotiques ?
Dans la plupart des cas, une monothérapie suffit. L’association d’antibiotiques vise essentiellement trois objectifs :
- Elargissement du spectre ;
- Synergie ;
- limitation du risque de résistance bactérienne.
Dans la pratique la synergie entre deux antibiotiues est mesurée en incubant les bactéries en présence de différentes concentrations (différentes dilutions) des antibiotiques concernés.
Ondit que deux antibiotiques sont synergiques lorsque les concentrations des antibiotiques associés nécessaires pour inhiber la croissance des bactéries sont réduites à ≤25% de leur CMI. Tout se passe comme si un des AB agit en rendant les germes plus sensibles à l’autre. L’effet de l’association est supérieur à la somme des effets des deux antibiotiques.
On dit que l’effet est « additif » lorqu’en association les concntrations nécessaires pour inhiber la croissance des bactéries sont outour de 50% de la CMI. L’effet de l’association est égal à la somme des effets des deux antibiotiques. Ceci suggère que les deux antibiotiques agissent indépendament l’une de l’autre.
Si les concentrations nécessaires pour inhiber la croissance bactérienne par deux antibiotiques associés sont cupérieurs à 50% de la CMI, on dit qu’il y a « antagonisme ». L’effet de l’association est inférieur à la somme des actions des deux antibiotiques. Les antibiotiques bactériostatiques exercent un effet antagoniste sur les bactéricides. En effet, ils réduisent la division cellulaire ou la synthèse desprotéines qui sont nécessaire pour l’action des bactéricides. Il est ainsidéconséillé d’associer des bactéricides aux bactériostatiques.
Il existe des situations pour lesquelles l’association d’antibiotique s’impose :
- Pour certains germes comme le Bacille de Koch (TBC), le pseudomonas, et en général les bacilles Gram négatifs, pouvant acquérir de la résistance chromosomique (par mutation)
- Certains sites infectieux imposent aussi une association d’antibiotiques soit parce qu’ils sont difficiles d’accès soit parce que les infections y sont souvent plurimicrobiennes: endocardite, infection neuroméningée post-chirurgicale, infection intrapéritonéale, infection pelvienne non documentée, staphylococcie grave.
- L’état du patient peut aussi imposer l’association : patient en état grave, neutropénique
- Les infections nosocomiales, souvent causés par des germes résistants, ou multi résistants, se traiteront de préférence par des associations d’antibiotique
- Enfin, certains antibiotiques, en raison du risque d’automutation, ne devraient pas être utilisés seuls ; ils doivent être associés à d’autres : rifampicine, fosfomycine, acide fucidique
Il faut veiller à associer des antibiotiques dont la Pharmacocinétique est telle qu’ils atteignent tous des concentrations efficaces au site d’infection. Une association de deux antibiotiques dont l’un ateint le site infectieux à des concentrations efficace mais pas l’autre est appelés « fausse association ».
Eviter les associations d’antibiotiques à même site d’action ou antagonistes. L’association de bactéricides avec les bactériostatiques s’est avérée être antagoniste.
Antibiotiques antagonistes : Cyclines + penicilline ; Rifampicine + pénicilline ou vancomycine
5. Quelle posologie ?
Chaque fois que possible, les posologies seront en mg/Kg, y compris chez l’adulte. La posologie est indépendante du niveau de gravité de l’infection pour les aminosides, glycopeptides, tétracyclines, macrolides. La posologie est adaptée à la gravité de l’infection et à la sensibilité présumée du germe pour les bétalactamines, car leur efficacité est “temps dépendante”, leur diffusion assez faible (notamment dans le LCR) et leur marge thérapeutique large. Il en va de même pour les fluoroquinolones. Une dose forte initiale, dite “dose de charge”, peut être indiquée pour les aminosides, car leur efficacité est “concentration dépendante”, et pour certains antibiotiques à demi- vie longue comme la téicoplanine afin d’obtenir plus rapidement l’état d’équilibre.
6. Recours à la chirurgie ?
Il est obligatoire dans toutes les s de suppuration ou d’obstruction canalaire. Dans ce cas, l’évacuation du pus ou la levée de l’obstacle seront nécessaires.
7. Quelle voie d’administration ?
Il faut tenir compte des voies d’administration des antibiotiques et des possibilités d’absorption du patient et de l’urgence. La voie IV et celle des urgences et des infections graves. Pour la voie orale, s’assurer de l’intégrité du tube digestif.
8. Quel rythme d’administration ?
Le rythme tiendra compte des propriétés pharmacocinétique et pharmacodynamique (PK/PD) des antibiotiques.
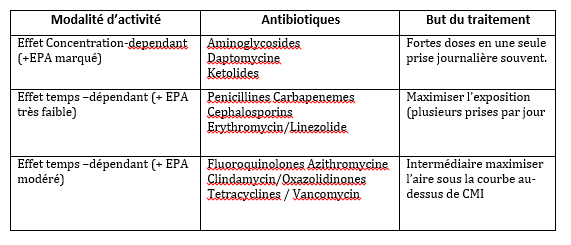
Certains antibiotiques sont rapidement bactéricides avec effet post-antibiotique important (l’activité bactéricide demeure présente même quand les concentrations de l’aantibiotique sont descendues au-dessous de la CMI.). Ce sont des antibiotiques à effet concentration-dépendant
Pour d’autres antibiotiques l’effet est lent. Ils sont lentement bactéricides. Le facteur déterminant de leur efficacité est le temps pendant lequel les concentrations sont restées au-dessus de la CMI. Ce sont des antibiotiques à effet temps-dépendants.
Pour les antibiotiques à activité concentration dépendante (aminosides), de fortes doses en une ou deux administrations par jour seront nécessaires. Les posologies restne les êmes quelle que soit la gravité de l’infestion. Ex : gentamicine, chez l’adulte la posologie recommandée est de 160mg en une prise plutôt que 2x80mg. L’administration en une seule forte dose est plus efficace et même moins toxique (néphrotoxicité moindre).
Pour les antibiotiques à activité temps dépendante, il sera nécessaire de procéder à plusieurs administrations : 3 à 6 par jour. Les posologies augmentent en fonction de la gravité de l’infection ; et cette augmentation se fait en multipliant le nombre de prises plutôt qu’en augmentant les doses par prise. Ex : pour la cefotaxime, On passera ainsi de 3X2gr à 4x2gr et même 6x2gr !
1. Quelle durée de traitement ?
Prolonger une antibiothérapie au-delà de 10 jours n’est pas justifié en termes d’efficacité dans la majorité des infections, et augmente le risque d’émergence de résistance parmi les bactéries des flores commensales. Il existe une corrélation positive entre la durée de l’antibiothérapie et le risque d’émergence de résistances.
Pour certains antibiotiques toxiques, la durée doit être réduite le plus possible (maximum 5 jours pour les aminosides, sauf quelques exceptions comme le cas d’endocardite bactérienne pour laquelle on peut les administrer pendant 14 jours au plus)
Surveillance de l’antibiothérapie
Toute antibiothérapie doit être surveillée après son instauration. Il faudra surveiller l’efficacité de l’antibiotique et l’innocuité (effets indésirable)
La surveillance de l’efficacité se fait en observant l’ammandement des symtomes cliniques et biologiques ; la protéine-C réactive est un meilleur témoin d’efficacité car son taux diminue rapidement en cas de guérison ; la vitesse de sédimentation diminue trop lentement pour servir de témoin de guérison.
Toute antibothérapie devrait être ré-évaluée au 3ème, 4ème jour de traitement. L’antibiotique utilisé peut être alors:
- interrompu si le diagnostic d’infection bactérienne n’est pas confirmé ou semble très peu probable.
- poursuivie sans changement s’il est efficace, et bien toléré par le patient
- adaptée aux résultats bactériologiques et à l’antibiogramme: remplacement le plus souvent possible par un antibiotique à spectre étroit, moins susceptible de favoriser le développement de bactéries résistantes. C’est ce qu’on appelle la désescalade antibiotique.
- ajout d’un autre antibiotique pour élargir le spectre (infection plurimicrobienne) ou renforcer la bactéricidie en cas de monothérapie initiale (staphylocoques, P. aeruginosa, germe multirésistant responsable d’une infection nosocomiale)
- radicalement modifiée en cas d’inefficacité, en changeant de classe d’antibiotiques ou en choisissant des antibiotiques plus performants dans la même classe.
Fièvre sous antibiothérapie
Un patient qui fait de la fièvre malgré l’antibiothérapie pose de sérieux prolèmes à l’équipe soignante. Deux situations :
- la fièvre perdure malgré le traitement antibiotique ou bien
- la fièvre a baissé puis remonte malgré la poursuite de l’antibiothérapie. Plusieurs cas de figue sont à envisager :
1. Cause non directement en rapport avec l’infection initiale:
- Infection non bactérienne: virale, parasitaire, mycosique.
- Fièvre non infectieuse: fièvre d’origine immuno-allergique (sensibilisation à l’antibiotique), maladie thrombo-embolique sous-jacente,
- affections sous-jacentes initiatrices de l’infection telles: hémopathies, cancers, collagénoses.
- Complications de l’antibiothérapie à type de thrombophlébite suppurée sur cathéter, abcès de fesse dû aux infections intramusculaires, colite pseudomembraneuse.
2. Echec de l’antibiothérapie
On distingue essentiellement 3 causes d’échec
- Cause microbiologique: erreur sur le germe en cause, méconnaissance d’une association de germes, sélection de mutants résistants, surinfection.
- Cause pharmacocinétique: posologie insuffisante, mauvaise absorption digestive, mauvaise difusion au site de l’infection, inobservance du traitement, durée de traitement trop courte, interactions métaboliques, interactions médicamenteuses.
- Causes diverses: foyer enclos nécessitant un geste chirurgical, infection sur matériel étranger, traitement insuffisant de la porte d’entrée.
La conduite sera différente selon quel’agent causal a été identifié (antibiothérapie documentée) ou juste supposé (antibiothérapie probabiliste).
En cas d’antibiothérapie probabiliste
Plusieurs questions se posent du fait que le germe en cause n’a pas été formellement identifié :
- S’agissait-il d’une infection bactérienne ? (Une embolie pulmonaire peut mimer une pneumopathie résistante aux antibiotiques. Les maladies de système à point de départ pulmomaire ou ORL (maladie de Wegener…) peuvent débuter par une fièvre.
- Et si c’était une infection bactérienne, le germe est-il sensible à l’antibiotique utilisé ? Avant toute discussion, bien s’assurer de l’observance et de la tolérance du traitement. Les échecs peuvent être dus à la non-compliance ou à des problèmes pharmacologiques
Conduite à tenir:
- Il faudra modifier l’antibiothérapie selon le consensus établi: par exemple devant une pneumopathie du sujet sain sans signe de gravité, on passe d’une aminopénicilline à un macrolide
- Il faut tenter de documenter l’échec: faire une fenêtre thérapeutique (arrêt de l’antibiotique initial pendant 48-72 heures) à condition qu’il n’y ait pas d’urgence thérapeutique. Ensuite, il faudra tenter d’isoler la bactérie responsable en faisant des prélévements au site de l’infection.
- Il faut remettre en cause le diagnostic initial si la modification thérapeutique n’a pas été efficace et s’il n’a pas été possible d’isoler un germe:
En cas d’antibiothérapie documentée
Il s’agira ici d’un échec thérapeutique dont les causes sont diverses :
1. Echec lié à l’hôte
Mauvaise compliance, interruption de traitement pour diverses causes (effets indésirables, inconfort…). Mauvaise prise de médicament (suspension : mauvaise dilution ou manque de mélange le médicament reste concentré dans le dépôt au fond du verre avec pour conséquence des sous- dosages.
2. Echec de cause pharmacologique
- Modification de l’absorption digestive
- diarrhée, vomissements
- alimentation: certains aliments perturbent l’absorption des antibiotiques (les produits laitiers avec les cyclines). D’autres au contraire voient leur absorption augmentée par le repas: céfuroxine axétil, cefpodoxime proxétil…
- Dosage insuffisant pour le patient: non adapté au poids, ou diminué volontairement par lui.
- Association médicamenteuses antagonistes
- la biodisponibilité de l’antibiotique peut être modifiée par d’autres produits pris en même temps, par exemple: les antiacides, les anti-H2, le kétoconazole et le fluconazole diminuent l’absorption de la rifampicine
- l’accélération du métabolisme hépatique par des inducteurs enzymatiques comme la rifampicine ou le phénobarbital nécessite l’augmention de la posologie journalière des antibiotiques à métabolisme hépatique et la diminution de l’intervalle entre les prises.
- Diminution des concentrations sériques et tissulaires
- par une augmentation du volume de distribution chez la femme enceinte, les insuffisants rénaux, lors des états septiques graves, chez les patients de réanimation à l’état hémodynamique ou d’hydratation instable et chez les sujets neutropéniques fébriles
- par diminution de l’absorption digestive chez l’obèse par fixation lipidique des antibiotiques lipophiles.
- Intervalle trop grand entre les administrations, laissant aux bactéries survivantes le temps de se multiplier à nouveau.
- Mauvaise pénétration tissulaire principalement dans le LCR et l’encéphale, dans l’os, la prostate, l’oeil, les végétations d’endocardite et les abscès ou les pleurésies enkystées: antibiotique mal choisi par rapport au site de l’infection.
- Conditions locales défavorables elles réduisent l’activité des antibiotiques: pH, anaérobiose… (aminosides) elles rendent nécessaire un drainage chirurgical du foyer.
3. Echec de cause bactériologique
- Germe résistant à l’antibiotique. il faut alors modifier le traitement, selon l’antibiogramme.
- Effet inoculum : certains antibiotiques notamment ceux à activité temps dépendante ont une activité réduite lorsque la quantité de bactéries est importante (bétalactamines sauf l’imipénème). Les antibiotiques à activité concentration dépendante ne sont pas affectés par l’effet innoculum. (aminosides, les fluoroquinolones)
- Pathogénie indirecte bactérienne lorsque par exemple, la flore commensale de l’organe infecté contient une bactérie productrice d’enzymes pouvant inactiver l’antibiotique (pénicillinase produite par un staphylocoque commensal de la gorge).
- Association antagoniste d’antibiotiques.
